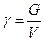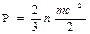Основными параметрами характеризующими термодинамическое состояние жидкости являются
Основные термодинамические параметры состояния.







Основные термодинамические параметры состояния.
In рассматривается паровой двигатель, процесс легкого перемещения рабочей жидкости из парового состояния в жидкое и, наоборот, из жидкого в паровое состояние. характеризующими это состояние. Это называется параметром состояния в термодинамике.
Физическое состояние организма полностью определяется несколькими величинами Людмила Фирмаль
Параметры состояния имеют ряд преимуществ, включая удельный объем, давление, температуру, внутреннюю энергию, энтальпию, энтропию, концентрацию и изометрический потенциал. Однако при отсутствии силового поля (гравитации, электромагнетизма и др.), состояние однородного тела можно однозначно определить по 3 параметрам, которые используются в технической термодинамике как определенный объем, абсолютная температура и давление.
Эти 3 параметра, обычно называемые базовыми, не являются независимыми величинами, а связаны между собой четко определенными математическими зависимостями, как показано ниже. Удельный объем. Удельный объем однородного вещества-это объем, занимаемый единицей массы вещества. В технической термодинамике удельный объем обозначается V и измеряется в м3 / кг. в = ВИМ、
В тепловом двигателе так называемая рабочая жидкость используется для преобразования тепла в работу. Например, не только газотурбинная установка, но и двигатель внутреннего сгорания учитывает процесс, в котором рабочим телом является gas. In рассматривается паровой двигатель, процесс легкого перемещения рабочей жидкости из парового состояния в жидкое и, наоборот, из жидкого в паровое состояние.
Физическое состояние организма полностью определяется несколькими величинами, характеризующими это состояние. Это называется параметром состояния в термодинамике. Параметры состояния имеют ряд преимуществ, включая удельный объем, давление, температуру, внутреннюю энергию, энтальпию, энтропию, концентрацию и изометрический потенциал.
Однако при отсутствии силового поля (гравитации, электромагнетизма и др.), состояние однородного тела можно однозначно определить по 3 параметрам, которые используются в технической термодинамике как определенный объем, абсолютная температура и давление. Эти 3 параметра, обычно называемые базовыми, не являются независимыми величинами, а связаны между собой четко определенными математическими зависимостями, как показано ниже.
Удельный объем. Удельный объем однородного вещества-это объем, занимаемый единицей массы вещества. В технической термодинамике удельный объем обозначается V и измеряется в м3 / кг. в = ВИМ、 Где V-объем любого количества вещества,/ m p0, atomic pv> p0«.
Под влиянием перепада давления px-p0 жидкость в правом колене поднимается и уравновешивает избыточное давление в сосуде. Фто = Р * Ф + hFpg. Откуда ч = р± = л£
Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ СОСТОЯНИЯ
В термодинамике существует также деление параметров на термические (давление, температура, объем) и калорические (удельная энергия, удельная теплоемкость, удельные скрытые теплоты фазовых переходов).
Для характеристики конкретных условий, в которых находится данная система, или процесса, идущего в системе, необходимо прежде всего знать такие внутренние параметры состояния, как удельный объем, абсолютное давление, абсолютная температура.
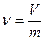
Величина, обратная удельному объему, называется плотностью (ρ, кг/м 3 );
Плотность это масса вещества, содержащаяся в единице объема или другими словами, масса единицы объема жидкости называется плотностью
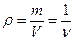
Масса и вес связаны между собой отношением
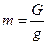
с учетом [3] получим соотношение между удельным весом и плотностью
Р = 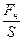
В соответствии с молекулярно-кинетической теорией давление газа рассматривается как результат ударов молекул о стенки сосуда и определяется соотношением [5]
где n — число молекул в единице объема; m — масса молекулы; с 2 — средняя квадратичная скорость поступательного движения молекул.
Согласно Международной системе единиц (СИ) удельное давление замеряют в Ньютонах на один квадратный метр (Н/м 2 ). Эта единица измерения давления называется Паскалем (Па). Один мегапаскаль равен 10 6 Па (1 МПа = 10 6 Па).
Термодинамическим параметром состояния является только абсолютное давление, которое отсчитывается от абсолютного нуля давления или абсолютного вакуума.
Для измерения давления в технике применяют приборы, измеряющие не абсолютное (полное) давление (Рабс), а разность между абсолютным и атмосферным (барометрическим) давлением Ратм.
Приборы, применяемые для измерения давлений, больших атмосферного, называются манометрами. Они показывают избыток давления измеряемой среды над атмосферным (манометрическое давление). Для измерения давлений меньших атмосферного, применяют вакуумметры, которые показывают, насколько абсолютное давление окружающей среды меньше атмосферного. Эту недостачу давления до атмосферного называют вакуумом.
При замере давлений жидкостными приборами вследствие расширения жидкости при нагревании ее объем увеличивается и, следовательно, увеличивается столб жидкости, что приводит к неправильным показаниям приборов. При таких замерах необходимо высоту столба жидкости приводить к 0 °С. Это приведение производится по формуле
где h0— показания барометра (манометра), приведенные к 0 °С; h— высота столба жидкости, наблюдаемая при t °С; α — объемный коэффициент расширения жидкости (для ртути α — 0,000172).
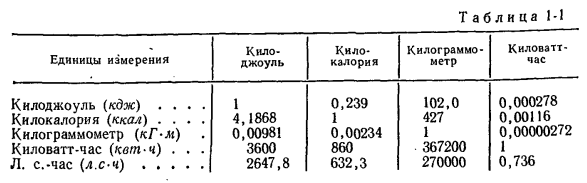
В технике применяется достаточно большое число единиц измерения давления. Соотношения между ними приведены в таблице [5].
Температура.Температура любого тела — величина, характеризующая степень нагретости тела, и представляет собой меру интенсивности «теплового движения» молекул. Таким образом, температура представляет собой меру средней кинетической энергии поступательного движения его молекул, т. е. температура характеризует среднюю интенсивность движения молекул, и чем больше средняя скорость движения молекул, тем выше температура тела. Понятие температуры не может быть применено к одной или нескольким молекулам. Если два тела с различными средними кинетическими энергиями движения молекул привести в соприкосновение, то тело с большей средней кинетической энергией молекул (с большей температурой) будет отдавать энергию телу с меньшей средней кинетической энергией молекул (с меньшей температурой), и этот процесс будет протекать до тех пор пока температуры средних кинетических энергии молекул обоих тел не сравняются, т.е. не выровняются температуры обоих тел. Такое состояние двух тел называется тепловым равновесием
Другими словами если две системы находятся в тепловом контакте, то в случае неравенства их температур они будут обмениться теплотой друг с другом, если же их температуры равны, то теплообмена не будет.
С точки зрения молекулярно-кинетических представлений температура есть мера интенсивности теплового движения молекул. Ее численное значение связано величиной средней кинетической энергии молекул вещества:
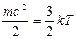
В отличие от стоградусной шкалы, применявшаяся ранее шкала Цельсия имела те же постоянные точки, соответствующие таянию льда при 0° и кипению воды при 100°, но равномерные деления.
В абсолютной термодинамической шкале Кельвина за нуль принято состояние тела, при котором тепловое движение молекул теоретически отсутствует. Из физики известно, что такое состояние наступает при температуре на 273° С (273,16°) ниже 0° С. Абсолютная температура всегда величина положительна.
Величина градуса по шкале Кельвина принимается равной градусу по стоградусной шкале: 1° К= 1°С; следовательно, ΔT = Δ t.
Соотношение между температурой, измеренной по абсолютной и стоградусной шкале:
0°К = —273° C; 0°С = + 273°К; Т° К = t° С + 273°; Т = —20 0 С = 253 0 К
Параметром состояния газа является абсолютная температура Т° К.
Основные термодинамические параметры состояния
Каждое равновесное состояние (см. параграф 1.3) термодинамической системы характеризуется определенными физическими величинами — равновесными параметрами состояния. Внутренние параметры характеризуют внутреннее состояние системы. К ним относятся давление, температура, объем и др. Внешние параметры характеризуют положение системы (координаты) во внешних силовых полях и ее скорость.
Внутренние параметры в свою очередь подразделяются на интенсивные и экстенсивные. Интенсивные — это те параметры, величины которых не зависят от массы тела (давление, температура, удельный объем, удельная теплоемкость). Экстенсивные — это те параметры, величины которых зависят от количества вещества в системе (объем, масса и др.).
В термодинамике существует также деление параметров на термические (давление, температура, объем) и калорические (удельная энергия, удельная теплоемкость, удельные скрытые теплоты фазовых переходов).
Для характеристики конкретных условий, в которых находится данная система, или процесса, происходящего в системе, необходимо прежде всего знать такие внутренние параметры состояния, как удельный объем, абсолютное давление, абсолютная температура.
Удельный объем v (м 3 /кг) — это объем единицы массы, т.е. величина, определяемая отношением объема к его массе:
где V— объем произвольного количества вещества (м 3 ); т — масса этого вещества (кг).
Величина, обратная удельному объему, называется плотностью р (кг/м 3 ). Плотность — это масса вещества, содержащегося в единице объема:
Давление — величина, определяемая отношением силы (нормальной составляющей силы), действующей на поверхность, к площади этой поверхности (Па = Н/м 2 ):
где F„ — нормальная составляющая силы (Н); S — площадь поверхности, нормальной к действующей силе (м 2 ).
Согласно Международной системе единиц (СИ) удельное давление замеряют в ньютонах на один квадратный метр (Н/м 2 ). Эта единица измерения давления называется паскалем (Па). Один мегапаскаль равен 10® Па (1 МПа = 10 6 Па).
До настоящего времени в технике используется также «старая» единица измерения удельного давления — техническая атмосфера (ат), представляющая собой силу в 1 кгс, действующую на 1 см 2 площади.
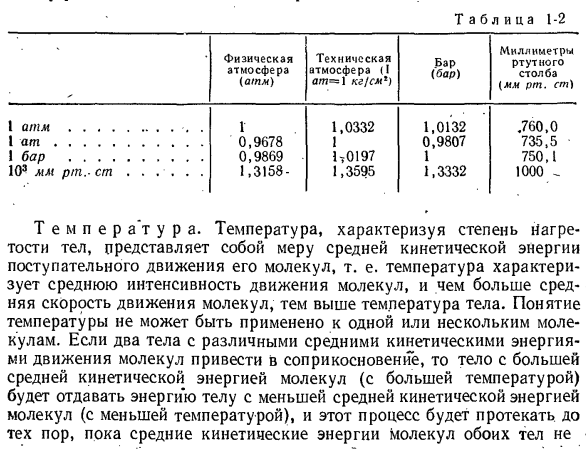
Различают давления атмосферное, избыточное и разрежение (вакуум). Атмосферным называется давление атмосферного воздуха на уровне моря. За единицу атмосферного давления принимается давление столба ртути высотой 760 мм (одна физическая атмосфера обозначается «атм»). Таким образом, 1 атм = 760 мм рт. ст.
Термодинамическим параметром состояния является только абсолютное давление, которое отсчитывается от абсолютного нуля давления, или абсолютного вакуума.
Для измерения давления в технике используют приборы, показывающие не абсолютное (полное) давление, а разность между абсолютным и атмосферным (барометрическим) давлениями. Приборы, применяемые для измерения давлений, больших атмосферного, называются манометрами. Они показывают избыток давления среды над атмосферным (манометрическое давление). Для измерения давлений, меньших атмосферного, используют вакуумметры, которые показывают, насколько абсолютное давление окружающей среды ниже атмосферного. Эту величину, показывающую недостачу давления до атмосферного, называют вакуумом.
Если давление газа в емкости больше атмосферного (рис. 1.1, а), то в точках с и d левого и правого колена трубки давления будут одинаковыми, так как жидкость находится в равновесии, а точки с и Улежат на одном уровне. Условие равновесия сил относительно уровня cd записывается в виде
где F = plxS — сила давления газа на жидкость в трубке в точке с; Fj = PCyS — сила давления атмосферного воздуха на жидкость в трубке в точке /; F2 = рghS — сила давления столба жидкости высотой h в точке d (вес столба жидкости высотой h).
Подставляя формулы для сил давления в условие равновесия, получаем
где ра — абсолютное (полное) давление газа в емкости; р^ — атмосферное (барометрическое) давление по барометру; р — плотность жидкости в мано-
Рис. 1.1. Измерение давления газа
После сокращения на S получаем
где у = рg — удельный вес манометрической жидкости; уА = ры — манометрическое давление столба жидкости высотой А, выраженное в тех же единицах, в каких даны давления рл и р(у
Если давление в емкости меньше атмосферного, то условие равновесия сил, действующих на жидкость в манометре, относительно уровня cd будет иметь вид (рис. 1.1, б)
где ри = pgA — давление, создаваемое столбом жидкости высотой А.
Это давление определяет вакуум в резервуаре. То есть вакуумом называют недостачу давления ра в емкости до атмосферного.
Избыточное давление и вакуум не являются параметрами состояния, так как они при одном и том же абсолютном давлении могут принимать различные значения в зависимости от величины атмосферного давления.
В технике применяется достаточно большое число единиц измерения давления. Соотношения между ними приведены в табл. 1.1.
Техническая атмосфера, ат (кгс/см 2 )
Миллиметры ртутного столба, мм рт. ст.
Миллиметры водного столба, мм вод. ст.
1 мм вод. ст. (1 кгс/м 2 )
При замере давлений жидкостными приборами вследствие расширения жидкости при нагревании ее объем увеличивается и, следовательно, увеличивается столб жидкости, что приводит к неправильным показаниям приборов. При таких замерах необходимо высоту столба жидкости приводить к 0°С. Это приведение производится по формуле
где А0 — показания барометра (манометра), приведенные к 0°С; А — высота столба жидкости, наблюдаемая при ГС; а — объемный коэффициент расширения жидкости (для ртути а = 0,000172).
В настоящее время используются две температурные шкалы.
Между температурами, выраженными в Кельвинах и градусах Цельсия, имеется соотношение
В так называемой тройной точке, где жидкая, твердая и газообразная фазы находятся в устойчивом равновесии, температура в Кельвинах равна Т = 273,16 К, а в градусах Цельсия t = 0,01°С.
Параметром состояния является абсолютная температура, выраженная в Кельвинах, по градус абсолютной шкалы численно равен градусу шкалы Цельсия, так что dT = dt.
Температура тела (Г, К) — величина, характеризующая степень нагрето- сти тела. Она представляет собой меру средней кинетической энергии поступательного движения молекул. Чем больше средняя скорость движения молекул, тем выше температура тела.
Взаимосвязь между средней кинетической энергией поступательного движения молекул mze 2 /2 и абсолютной температурой идеального газа Т описывается соотношением
где m — масса молекулы; w — средняя квадратичная скорость поступательного движения молекул; k = 1,38 • 10
Термодинамика
Лекция 1. Предмет технической термодинамики и ее методы
1. Предмет термодинамики
2. Основные параметры состояния тела
3. Понятие о термодинамическом процессе
4. Гомогенные и гетерогенные термодинамические системы
5. Термодинамическое равновесие
1. Предмет термодинамики
Термодинамика наука о превращениях различных видов энергии из одного в другой, и о наиболее общих макроскопических свойствах материи. Она изучает различные как физические, так и химические явления, обусловленные превращениями энергии. Применение закономерностей термодинамики позволяет анализировать свойства веществ, предсказывать их поведение в различных условиях. Термодинамика дает возможность исследовать различные процессы от простых в однородных средах до сложных с физическими и химическими превращениями, биологических и др.
Слово «термодинамика» происходит от греч. «therme» – тепло и «dynamis» – сила. Название науки возникло в период ее основания – в начале XIX в. В настоящее время слово «термодинамика» трактуют так: наука «о силах, связанных с теплотой».
Термодинамика основана на двух, экспериментально установленных законах (началах).
Первый закон (начало) является по существу законом преобразования и сохранения энергии применительно к процессам, изучаемым в термодинамике; невозможен процесс возникновения или исчезновения энергии.
Второй закон (начало) – определяет направление течения реальных (неравновесных) процессов; невозможен процесс, имеющий единственным своим результатом превращение теплоты в работу.
Термодинамический метод исследования основан на законах (началах) термодинамики и представляет собой их логическое и математическое развитие.
Объект исследования в термодинамике называют термодинамической системой или, в простом случае, термодинамическим телом. Одна из особенностей метода термодинамики состоит в том, что система (тело) противопоставляется всем другим телам, которые называют окружающей средой. Термодинамика построена дедуктивно: частные выводы получены из общих законов (начал).
Принято разделять термодинамику на физическую, или общую, химическую и техническую.
Физическая термодинамика разрабатывает метод термодинамики и применяет его для изучения фазовых превращений термоэлектрических и магнитных явлений, излучения, поверхностных явлений и т. п.
Химическая термодинамика изучает процессы с физическими и химическими превращениями с помощью метода термодинамики.
Техническая термодинамика устанавливает закономерности взаимного преобразования теплоты и работы, для чего изучает свойства газов и паров (рабочих тел) и процессы изменения их состояния; устанавливает взаимосвязь между тепловыми, механическими и химическими процессами, протекающими в тепловых двигателях и холодильных установках. Одна из основных ее задач – отыскание наиболее рациональных способов взаимного превращения теплоты, и работы.
Основные термодинамические параметры состояния
Каждое равновесное состояние (см. § 1.3) термодинамической системы характеризуется определенными физическими величинами — равновесными параметрами состояния. Внутренние параметры — давление, температура, объем и др. — характеризуют внутреннее состояние системы, внешние — ее положение (координаты) во внешних силовых полях и скорость.
Внутренние параметры, в свою очередь, подразделяются на интенсивные и экстенсивные. Значение интенсивных не зависит от размеров (массы) тела — это давление, температура, удельный объем (но не объем), удельная теплоемкость. Экстенсивные параметры зависят от количества вещества в системе — это объем, масса и др.
В термодинамике существует также деление параметров на термические (давление, температура, объем) и калорические (удельная энергия, удельная теплоемкость, удельные скрытые теплоты фазовых переходов).
Для характеристики конкретных условий, в которых находится данная система, или процесса, идущего в системе, необходимо прежде всего знать такие внутренние параметры состояния, как удельный объем, абсолютное давление, абсолютная температура.
Удельный объем (v, м 3 /кг) — это объем единицы массы, или величина, определяемая отношением объема к его массе:
где V — объем произвольного количества вещества, м 3 ; т — масса этого вещества, кг.
Величина, обратная удельному объему, называется плотностью (р, кг/м 3 ); или это есть масса вещества, содержащегося в единице объема:
Давление (р, Па) — величина, определяемая отношением силы (нормальной составляющей), действующей на поверхность, к площади этой поверхности:
Согласно Международной системе единиц (СИ) давление измеряют в ньютонах на квадратный метр (Н/м 2 ). Эта единица измерения давления называется паскалем (Па).
До настоящего времени в технике используют также «старую» единицу измерения давления — техническую атмосферу (ат), представляющую собой силу в 1 кгс, действующую на 1 см 2 площади:
Различают давления атмосферное, избыточное и разрежение (вакуум). Атмосферным называется давление атмосферного воздуха на уровне моря. За его единицу принято давление столба ртути высотой 760 мм (физическая атмосфера, атм). Таким образом, 1 атм = 760 мм рт. ст. Давление, которое больше атмосферного, называют избыточным, а меньше — разрежением. Для его измерения применяют манометры, барометры, вакуумметры.
Термодинамическим параметром состояния является только абсолютное давление, которое отсчитывается от абсолютного нуля давления или абсолютного вакуума.
В технике применяют приборы, измеряющие не абсолютное (полное) давление, а разность между абсолютным и атмосферным (барометрическим) давлением. Приборы, применяемые для измерения давлений, больших атмосферного, называются манометрами. Они показывают избыток давления измеряемой среды над атмосферным (манометрическое давление). Для измерения давлений, меньших атмосферного, применяют вакуумметры, которые показывают, насколько абсолютное давление окружающей среды меньше атмосферного. Эту недостачу давления до атмосферного называют вакуумом.
Если давление в емкости больше атмосферного (рис. 1.1, а), то в точках end левого и правого колена трубки давления будут одинаковыми, так как жидкость находится в равновесии, а точки с и Улежат на одном уровне. Условие равновесия сил относительно уровня cd записывается в виде
где F — сила давления газа на жидкость в трубке в точке с, F = paS; Fx — сила давления атмосферного воздуха на жидкость в трубке в точке f F <= pbS; F2 — сила давления столба жидкости высотой h в точке d (вес столба жидкости высотой h), F2 = рghS.
Подставляя формулы для сил давления в условие равновесия, получаем
Рис. 1.1. Схема измерения давления V-образным манометром
После сокращения на S получаем
где у — удельный вес манометрической жидкости, у = pg; у И — рм — манометрическое давление столба жидкости высотой h, выраженное в тех же единицах, в каких даны давления ра и р6.
Из формулы (1.4) следует, что рм = ра — pQ. Таким образом, манометром определяется избыток давления измеряемой среды над атмосферным.
Если давление в емкости меньше атмосферного, то условие равновесия сил, действующих на жидкость в манометре, относительно уровня cd будет иметь вид (рис. 1.1, б)
Отсюда ра= рь — рв, где рп — давление, создаваемое столбом жидкости высотой /г, рв = pgИ. Оно определяет вакуум в резервуаре, т.е. вакуумом называют недостачу давления ра в емкости до атмосферного.
Избыточное давление и вакуум не являются параметрами состояния, так как они при одном и том же абсолютном давлении могут принимать различные значения в зависимости от атмосферного давления.
В технике применяется достаточно много единиц измерения давления. Соотношения между ними приведены в табл. 1.1.
Единицы измерения давления
Физическая атмосфера, атм
Техническая атмосфера, ат (кгс/см 2 )
Миллиметры ртутного столба, мм рт. ст.
Миллиметры водного столба, мм вод. ст.
При замере давлений жидкостными приборами вследствие расширения жидкости при нагревании ее объем увеличивается и, следовательно, увеличивается столб жидкости, что приводит к неправильным показаниям приборов. При таких замерах необходимо высоту столба приводить к О °С. Это приведение проводится по формуле
где h0 — показания барометра (манометра), приведенные к О °С; h — высота столба жидкости, наблюдаемая при t °С; а — объемный коэффициент расширения жидкости (для ртути а = 0,000172).
Температура (Т, К) — величина, характеризующая степень нагре- тости тел. Она представляет собой меру средней кинетической энергии поступательного движения молекул. Чем больше средняя скорость движения молекул, тем выше температура тела.
Взаимосвязь между средней кинетической энергией поступательного движения молекул mw 2 /2 и абсолютной температурой идеального газа Т описывается соотношением
где m — масса молекулы; w — средняя квадратичная скорость поступательного движения молекул; къ — постоянная Больцмана, кБ = 1,38 • КГ 23 Дж/К.
В настоящее время используют две температурные шкалы.
Между температурами, выраженными в кельвинах и градусах Цельсия, имеется следующее соотношение
В так называемой тройной точке, где жидкая, твердая и газообразная фазы находятся в устойчивом равновесии, температура в кельвинах равна Т = 273,16 К, а в градусах Цельсия — t = 0,01 °С.
Параметром состояния является абсолютная температура, выраженная в кельвинах, но градус абсолютной шкалы численно равен градусу Цельсия, так что dT = dt.
Абсолютная температура — величина всегда положительная. При температуре абсолютного нуля (Т= 0 К = —273,15 °С) прекращается тепловое движение молекул. Абсолютный нуль температуры недостижим, так как тепловое движение молекул — неотъемлемый атрибут материи, и его прекращение приводит к нарушению закона ее сохранения.